健康状态下,人体免疫系统处于一种稳态,既能识别和杀伤外来细胞或者变异的细胞,又能制约这种杀伤力,避免杀伤太过而殃及健康的组织细胞,人体中又广泛存在具有免疫调节功能的间充质干细胞(MSC)。
从免疫细胞对MSC的作用出发,阐述MSC进入体内的归宿,解释了为何MSC并不是通过分化来发挥治疗作用,即使MSC具有体内分化的能力。
首先,MSC具有体内分化的能力。妊娠早期,羊胎儿的免疫系统尚未得到建立,将人骨髓MSC注射到胎羊体内,可以观察到人MSC在多个组织中存活长达13个月,而且观察到MSC能分化为软骨细胞、脂肪细胞、心肌细胞、骨髓基质细胞和胸腺基质细胞。但是13个月后就检测不到人MSC的存在,说明人MSC进入羊体内,依然被羊的免疫细胞所清除。
其次,由于MSC具有一定的免疫原性,所以不管是静脉注射还是局部注射的MSC,都避免不了迟早被机体免疫细胞清除的命运,所以需要多次反复注射才能获得较好的疗效。
免疫细胞对MSC的清除
在多种动物物种中已经观察到异基因MSC没法长期定植,包括鼠,狒狒,猪和恒河猴。不同动物模型都观察到了4周或更长时间的异体MSC的存活。然而,其他研究表明,与自体MSC相比,异体MSC输入人体后的存活率降低了。尽管MSC的存活时间相对较长(长达24天),但在大鼠接受异体MSC颅内注射的部位,中性粒细胞、单核细胞和T细胞数量增加。
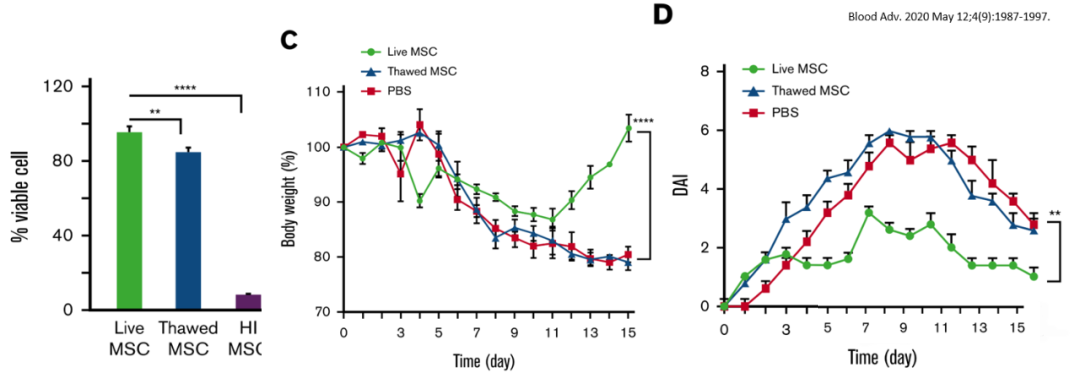
反复注射MSC产生抗体加速清除MSC
在猕猴颅内植入异体骨髓MSC后,出现循环中的白细胞、淋巴细胞和中性粒细胞的短暂但显著的增加,并在猕猴体内检测到循环中的同种抗体,但发现受体血清与补体介导的溶解无关。不仅是猕猴,在注射MHC不匹配的MSC的小鼠、大鼠、猪和马中也检测到同种抗体。未经处理和IFN-γ预处理的异体MSC,都能刺激健康大鼠注射异体MSC后产生供者特异性抗体。
静脉注射同种异体MSC可导致同种异体抗体的形成,这种抗体能够促进补体介导的针对MSC的溶解,伴随产生较低水平的IgM分泌。接种了不匹配的异体MSC的小鼠在第二次输注的24小时内表现出对供者来源的脾细胞的快速排斥反应。接受异体MSC腹腔注射的小鼠产生了高滴度的同种异体反应抗体,并排斥了随后的同种异体皮肤移植。
同样是心衰患者,10名患者中有4位接受异体脂肪局部注射治疗后,能检测到异体脂肪MSC的HLA-I类抗原的抗体。最近两项人MSC临床试验监测患者同种异体抗体的产生,发现虽然大多数患者在注射同种异体骨髓MSC后没有产生显著的同种异体抗体,但少数患者确实产生了同种异体抗体。

有趣的是,在猪的心肌梗死模型中,MSC诱导的同种抗体的产生可以通过联合应用免疫抑制剂钙调神经磷酸酶抑制剂他克莫司来预防。联合使用异体MSC输注和小剂量西罗莫司(雷帕霉素)治疗可以使MHC完全不相合的小鼠心脏移植获得长期存活。
将C57BL/6小鼠来源的表达EPO的MSC(EPO-MSC)接种于胶原支架内,皮下注射同遗传背景基因宿主(C57BL/6)或异基因宿主(BALB/c)宿主;作为MSC存活的指标,接受同基因EPO-MSC的小鼠的红细胞压积持续增加,而接受同种异基因EPO-MSC的小鼠的红细胞压积出现峰值,随后恢复到基线水平;而且植入15天后取出的胶原支架分析显示,CD8+T细胞和自然杀伤(NK)细胞仅在同种异体EPO-MSC移植物中有明显的浸润,并出现了针对EPO转基因MSC的抗体,加速了异基因EPO-MSC的清除(红细胞压积的峰值降低)。在另一项单独的研究中,将异基因EPO-MSC注射到具有免疫活性的宿主中,导致了对EPO抗原的增敏和抗EPO免疫反应。所以,不建议多次应用经过基因编辑的MSC,机体的免疫系统会识别到所编辑的基因,从而产生免疫应答反应,加速了MSC的清除。
马骨髓或脂肪组织来源的MSC通过静脉、动脉、腱内或眼内途径注射,89%的马在注射MSC后抗牛血清白蛋白(BSA)抗体呈阳性,但是抗BSA抗体的量与抗MSC抗体的产生没有相关性。此外,MSC的细胞表面可以结合补体,尽管补体对MSC功能的影响目前仍有争议,补体介导的MSC的裂解很可能依赖于同种抗体。
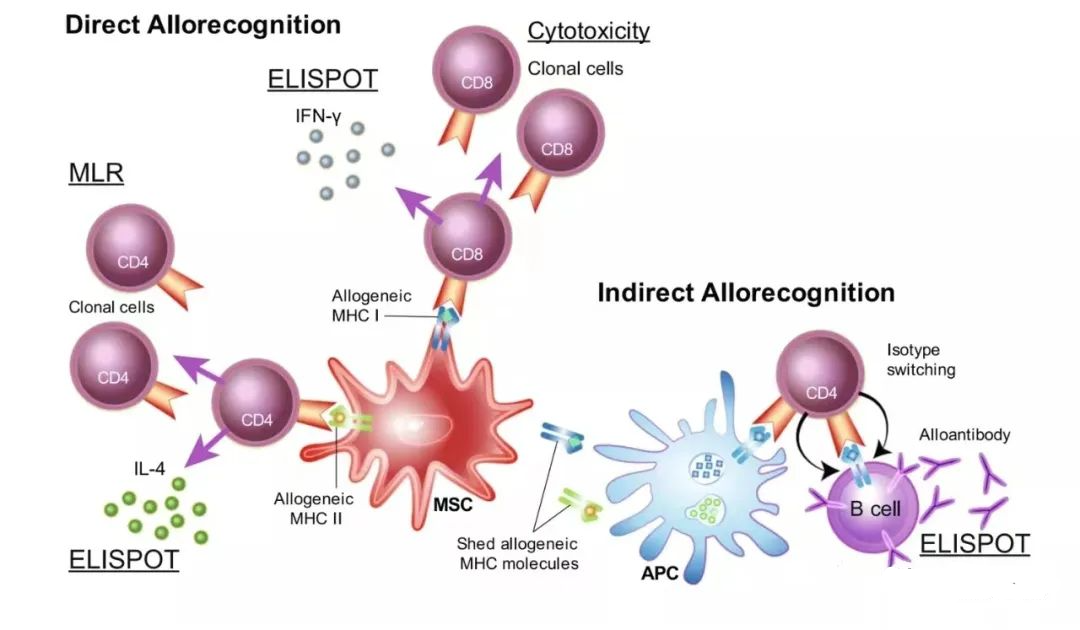
目前有许多标准的免疫学检测方法和技术可用于检测MSC的免疫原性。应该确定MHC单倍型,以了解供者或刺激者MSC与接受者或应答者细胞是完全不匹配还是部分不匹配。MSC的免疫调节功能可以用传统的MLR来衡量,即反应和刺激脾细胞或PBL与MSC共培养,但同种异体MSC抑制T细胞增殖的能力与同种异体MSC的体内免疫原性无关。单抗原珠(SAB)分析、ELISPOTS和HLA四聚体也被用于筛选人类血清中MHC特异性同种抗体,商业试剂盒也很容易买到。然而,这些检测并不能确定同种异体抗体的功能。
小结
综上所述,MSC不能被认为是真正的免疫豁免特权。MSC排斥的时间和严重程度依赖于MSC表达免疫原性和免疫系统之间的平衡决定。
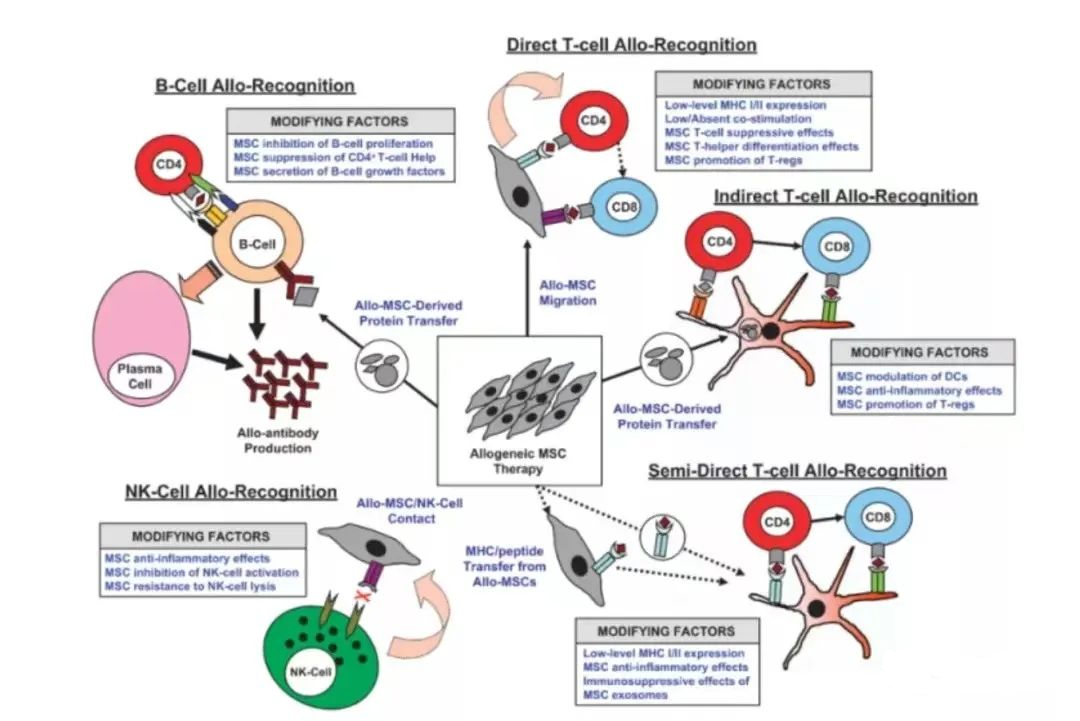
尽管如此,但是使用同基因(或自体)和异基因MSC的临床前模型和临床试验并未显示出与异基因MSC相关的不良事件。来自检测同基因和异基因MSC在伤口修复小鼠模型的数据表明,同基因和异基因MSC不会像同种异体成纤维细胞那样引起免疫反应。使用骨髓MSC治疗急性类固醇抗药性GVHD的2期临床试验的数据也表明,使用同种异体骨髓MSC不会触发免疫反应。甚至凋亡的MSC亦能降低盲肠穿孔导致肺和肾损伤大鼠的死亡率、血液中的TNF-α水平以及循环和脾脏T辅助细胞和细胞毒性T细胞(CTL)水平均显著降低。
总体而言,目前认为MSC具有在体内启动细胞免疫和体液免疫反应的能力,但由于固有的抗炎和免疫调节特性,与其他同种异体细胞相比,免疫原性的影响可能会大大减弱,从而整体上显示出了良好的治疗效果。这一点,在大量的临床应用研究的文献中得到了很好的证明,展示出MSC良好的治疗效果。
一句话总结MSC进入体内的命运:MSC在不断发挥治疗作用的同时,自己也被机体免疫细胞所识别和清除。
所以,MSC注射并非一劳永逸,临床研究需根据不同的适应症,适量、多次注射,或能达到理想的疗效。
MSC正如蜡烛:燃烧自己,照亮别人!



