近期,在美国糖尿病协会(ADA)的年度科学会议上,制药公司Vertex再次公布了其在研干细胞产品VX-880治疗1型糖尿病的1/2期多中心、单臂、开放临床试验中首批两名患者的详细随访数据[1],引起不小轰动。

第一例患者是一名患有1型糖尿病40多年的64岁男性,治疗后9个多月,他的糖化血红蛋白(HbA1c)处于正常范围,已经无需使用任何外源性胰岛素。
第二例是一名患有1型糖尿病10.7年的35岁女性,治疗后5个月,胰岛素使用量减少了30%,血糖处于正常范围内的时间显著增加。值得一提的是,两名患者都只接受了VX-880目标剂量的一半。
VX-880是什么?
VX-880是近年来备受关注的一款干细胞治疗在研产品,是一种用于治疗1型糖尿病的同种异体干细胞,可分化成胰岛细胞,通过肝门静脉输注后可定居于肝脏,并分泌胰岛素,从而补充1型糖尿病患者胰岛素绝对缺乏的情况。
VX-880如何让患者告别胰岛素依赖?
两名1型糖尿病患者是该项临床试验的初步尝试,治疗前都经历了多次严重的低血糖发作,甚至在骑摩托车时因低血糖发作而发生车祸。两名患者的生活严重被1型糖尿病困扰,多种治疗手段均收效甚微,为了彻底摆脱疾病负担,他们接受了上述临床试验,虽然只接受了原计划VX-880目标剂量的一半,但其所取得的疗效却是令人振奋的。
VX-880治疗后可以观察到外源性胰岛素依赖显著减少。
患者1是一名64岁男性,其1型糖尿病病史已经40余年,在接受VX-880的干细胞衍生胰岛细胞疗法后,其胰岛素使用量呈断崖式下降,从治疗前的每天34个单位的胰岛素注射减少到第90天的2.6个单位。到第210天,他能够停用胰岛素,到第270天,他达到了胰岛素独立的正式标准。(下图为患者1 90天时相关指标变化)。
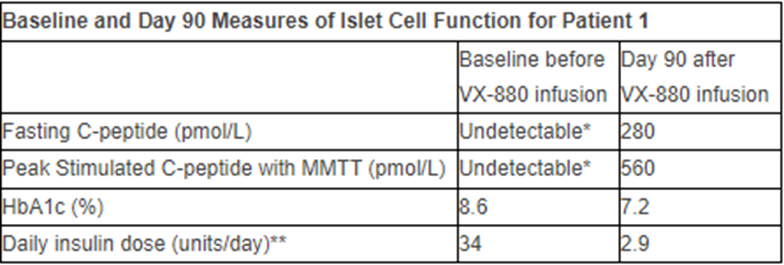
图片来自文献[2]
对于患者2,其患1型糖尿病10余年,VX-880治疗后胰岛素剂量也显著减少,从治疗前的每天25.9单位减少到第57天时的18.7单位,此后保持稳定,到第150天保持在18.2单位。
VX-880治疗后观察到内源性胰岛素产生明显增加。
C肽是除胰岛素外,另一项反映人体胰岛功能的重要指标,外源性使用胰岛素的患者,通常需要测C肽水平,因为其不受外源性胰岛素的影响,其值越高,表明内源性胰岛素分泌越多。
患者1和2在治疗前都检测不到C肽水平,表明其内源性胰岛素分泌功能极差。
治疗后90天,患者1空腹C肽为280 pmol/L,说明其已经恢复内源性胰岛素分泌,混合餐耐受试验(MMTT)刺激后其C肽峰值增加至560 pmol/L,表明治疗后其恢复了葡萄糖反应性胰岛素的产生。类似地,患者2的C肽水平随着随访时间的延长也在逐步恢复,在90天时增加到可检测的范围[1]。
FDA为干细胞治疗产品VX-880再开绿灯
VX-880疗法是当下最受关注的糖尿病干细胞疗法之一。 在2021年,该疗法相继通过了美国FDA的新药临床试验申请以及快速通道资格(FTD)。
不过这款疗法的临床发展道路也遭遇着不少的坎坷。尽管上述首批两名患者随访过程中的数据亮眼,出于对剂量增加后的安全性担忧,美国FDA在今年5月要求暂停该临床试验。
不过,近期又有了新进展,近日,FDA再次批准了该项临床试验继续进行。暂停的临床试验在两个月内能再次被批准进行的情况是不多见的,这也再一次证明了VX-880疗法过硬的安全性与疗效。
糖尿病的概况与干细胞治疗
根据国际糖尿病联合会(IDF)的数据[5],20-79岁之间的糖尿病患者已达到惊人的4.63亿人,占全球成年人口的9.3%,其中一半人没有意识到他们患有这种疾病,因此患严重相关并发症的风险更高。随着人口老龄化和肥胖率的增加,预计到2030年,患有糖尿病的成年人人数将增加到5.78亿人,如果不采取紧急行动,到2045年将跃升至惊人的7亿人。
虽然口服降糖药和胰岛素注射可以控制血糖,并可以预防并发症,但这只能达到对症治疗的目的,无法功能性治愈糖尿病。此外,这些药物存在大小不等的副作用。因此,迫切需要安全有效的替代疗法来对抗糖尿病。
目前,基于干细胞的治疗作为治疗糖尿病和减轻其并发症的一种可能的替代方法有着巨大的前景。
其中间充质干细胞(MSCs)是目前正在研究的治疗糖尿病的最有吸引力的成体干细胞类型。其具有自我更新能力、多潜能、抗原性低、归巢能力强、毒性低、易于体外培养和扩增等优点而备受关注。此外,它们含量丰富,可以很容易地从不同的组织中分离出来,包括骨髓、脂肪组织、脐带以及胎盘等。
间充质干细胞治疗糖尿病的全球概况
2021年,《细胞生物学与转化医学》(Cell Biology and Translational Medicine)发表综述阐述了间充质干细胞在糖尿病领域的应用,并表示,间充质干细胞因其独特的再生和免疫调节特性而被广泛应用于多个领域。

研究发现[5],间充质干细胞能够分化为胰岛样细胞或功能性胰岛素产生细胞(IPC),能够诱导内源性胰岛β细胞再生,并通过免疫调节特性保护这些细胞。此外,MSCs可能通过细胞-细胞直接接触或干细胞分泌体提供有利的胰腺微环境来激活内源性前体干细胞。
在过去的10年中,有几十项MSCs治疗糖尿病临床试验登记注册,占所有试验的6%(如下图所示)。其中大多数(51项)处于早期阶段(I期、I/II期或II期)。只有很少的第三阶段试验已经完成或正在进行。
这些研究中使用的MSCs大多来自脐带(33%),其次是骨髓(28%)和脂肪组织(25%)(如下图所示)。不过,超过90%的这些试验都是小规模的,每次试验的参与者不到100人。因此未来仍需进行更大规模的临床试验来验证其安全性与疗效。
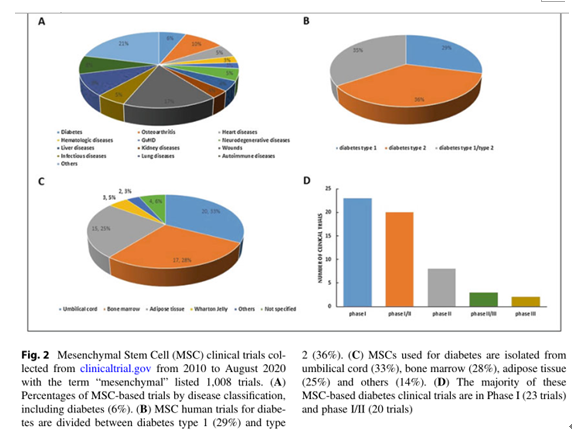
图片来自文献[5]
参考文献:
[1]https://www.medscape.com/viewarticle/975142#vp_1
[2]https://www.businesswire.com/news/home/20211018005226/en
[3]https://endpts.com/fda-lifts-hold-on-vertexs-diabetes-stem-cell-therapy-after-just-two-months-under-the-microscope/
[4]https://www.medscape.com/viewarticle/961696#vp_2
[5] Rifai L, Saleh FA. Conventional and Alternative Mesenchymal Stem Cell Therapies for the Treatment of Diabetes. Adv Exp Med Biol. 2021;1312:97-106.
https://pubmed.ncbi.nlm.nih.gov/33385177/




